摘要:所謂聞道有先后術業有專攻,創新藥本身就是涉及生物學,化學,臨床醫學等多學科前沿技術的產物。
盡職調查工作的本質是什么?是為了后續的決策提供信息,解決交易雙方的信息不對稱問題,并且盡可能的最大程度驗證信息的真實性與可靠性。創新藥領域的基礎投資邏輯是各個行業中最明確的,即通過解決病人的臨床需求來實現商業價值,若是再進一步則是通過專利保護來壟斷(請允許這樣說)某一時期內某些疾病的最優治療方法。
創新藥盡職調查工作也是圍繞上述邏輯來進行的,今天我們先談下項目創始團隊和商業價值的考量,后續幾期文章我們還會陸續分享項目實驗數據、專利分析等等其他盡調部分。

(盡調若排雷)
創始團隊和關鍵崗位人員
所謂聞道有先后術業有專攻,創新藥本身就是涉及生物學,化學,臨床醫學等多學科前沿技術的產物。對于一個創新藥公司的考察與評價完全區別去對人或其他行業公司的考察,只有當公司團隊集結了各方面極為資深的專業人士才能使項目順利推進。
通常來講一個成熟創新藥公司需要7種專業背景的人士通力配合才能保證項目的順利推進,這7各方面分別是生物學,化學,臨床,BD(商業拓展),知識產權,監管機構注冊申報和金融。在以上7個方面中知識產權,監管機構申報和金融方面可以通過外包來解決,例如聘用專業專利律所來布置專利整體架構撰寫權力要求,聘用CRO撰寫監管機構的申報材料,聘用FA或投行協助進行融資或上市等工作。而生物學,化學,臨床,BD(商業拓展)則是衡量一個公司實力的“硬指標”。當然上述要求也不是一成不變的,面對千變萬化的項目只有恰當的不斷調整才能讓盡職調查更好的為投資決策提供信息。例如當我們考察一個處于先導化合物篩選階段的項目,那么若該公司在臨床方面的能力有暫時性缺陷是可以容忍的。公司不同的技術路線也會影響對于公司團隊的考察點,假設目標公司是以全球首創靶點為目標依據靶點來開發新藥的企業,那么該公司的生物學核心人員的能力考察是重中之重。若是目標公司是使用經典藥物化學設計來改造生理反應已知的化合物進行藥物開發,那么生物學人員的考察就不再那么重要,重點考察對象將轉為對臨床候選化合物自身性質的研究。

(最佳7人組合)
除了團隊的完整性以外,公司靈魂人物(一般來說是公司創始人)的履歷永遠是盡職調查工作的重點。創新藥的研發是屬于少數精英的事業,如同投資行業一樣公司人數的多寡并不能客觀衡量一個公司的投資能力,同理一個創新藥研發公司的實力是由最核心的1到2個人的能力水平來決定的,而不是團隊的平均質量。正如前面所言創新藥是一個跨學科跨行業的領域,背景單一的創始人一般來說不能很好的勝任其工作,無論這個人在自身的專業領域多么出色。
這在我們過往的走訪經歷中一遍又一遍的驗證過,被調查公司的創始人有來自中國頂級院校教授、中組部國家千人計劃專家、美國常春藤大學教授、大型醫院著名醫生、全球大藥企的高管、藥品銷售公司創始人等。我們對于創始人的能力要求可以用一句話來概括“通百藝,而專一長”,即要求創始人在自身專業領域有極為過硬的造詣,同時對于新藥研發從選題立項到后期臨床乃至BD均有一定的經驗或了解,并且在公司需要時有儲備的各類專業人脈資源對接給公司。符合上述要求創始人的履歷通常是歐美大型制藥公司或者美國Biotech企業有超過20年項目經歷,至少做過附屬項目的主管,首席科學家甚至全球副總裁等職業履歷,并且主管的項目有進入臨床的記錄。

如果我們給目前最出色的創新藥企業家做一個畫像,典型形象大致是男性,年紀50歲出頭,80年代畢業于中國頂級學府,90年代留學歐美獲得博士學位,之后進入全球制藥巨頭或美國Biotech公司工作20年,擁有全流程的藥品開發經歷,2010年以后回國創業。可以說目前興起的創新藥開發熱潮是中國創新藥騰飛的第一個機會, 如果倒退10年根本不可能有足夠的人才做支撐,沒有這一批人才在工業界超過20年的積淀帶來的經驗與嚴謹創新藥的開發完全是空中樓閣。
當然,我們對團隊的考量維度還有更多,而且部分還是可以量化的。根據我們看了大量項目的實踐和不斷思考,我們也初步畫出了自己認知體系的邏輯思維導圖。當然這個是獨家IP,感興趣的朋友歡迎來我們辦公室喝茶暢聊。
臨床價值和商業價值
商業價值的考察可能是創新藥投資中最簡單也最復雜的一項,其簡單在于我們可以依據流行病學資料,售價,爬坡期,滲透率,專利期,專利結構,指南地位,競品數據,前一線療法的統計學結果等數據推算出潛在市場規模與項目估值,其復雜則在于我們需要考察資料背后的細節,這些細節有可能將帶給我們完全不同的故事。并且這些考察全部是根據項目定制化的,沒有任何規則可以套用。大量項目定制化的細節考察其本質就是不斷自我追問“有什么是我依然不知道的?”的過程。這不僅增加了盡職調查質量的不確定性,更加劇了盡職調查工作中最大的矛盾,即在盡調資源有限的情況下如何在保證盡職調查質量與在復數項目中調配資源之間取得平衡。
在談論創新藥的商業價值之前我們首先需要回到Biotech行業的基本邏輯,即創新藥發展的本質是解決未被滿足的臨床需求。而未滿足的臨床需求則是藥品的發展與疾病譜的變遷相互影響的結果: 一方面疾病譜的變遷導致創新藥向特定領域發展,另一方面創新藥的發展又使相關疾病被有效控制,從而改變了原有的疾病譜。
在過去的一百年中,由于科技與教育的飛速發展,讓人的壽命增長了整整30年。1940年代起各類抗生素的上市,使得天花、霍亂、鼠疫等曾經的不治之癥被有效控制;1970年代末期開始,普利類等降壓藥、他汀類等降脂藥、氯吡格雷等抗凝藥的陸續研發上市,使得絕大多數心腦血管疾病被有效控制。人類平均預期壽命向80歲邁進,同時惡性腫瘤,退行性神經病的發病率與死亡率逐步提高。藥品發展對于疾病譜的影響最典型的例子則是天花,在牛痘疫苗問世200年后,天花是世界上第一個被完全消滅的疾病。世界上最后一例自然天花病人在1977年出現于索馬里,隨后除了在1978年一名研究人員因為實驗室內因事故造成感染發病外全世界再無發病記錄。目前除了美國亞特蘭大疾控中心和俄羅斯國立研究所收藏的用于研究的冰凍病毒株外,自然環境下或許已無天花病毒的存在。

(大家都記住了琴納,卻沒人記住男孩的名字)
拋開歷史上的案例不談,疾病譜的變化在投資中對于藥品商業價值的判斷有著至關重要的意義。
例如A企業開發的主要產品聚焦于肝癌靶向藥,B公司則是開發肝癌手術用藥。如果僅僅表面性的認為癌癥是人類第二大死因而肝癌則是發病率排名前五的大癌種,在治療手段有限的情況下藥品一旦開發成功將有巨大的價值。因為靶向藥服藥期長于手術用藥,A的理論價值要高于B。但如果我們進一步分析則發現目前肝癌的發病原因中乙肝,丙肝,酒精性肝炎,非酒精脂肪型肝炎約占了發病原因的90%以上。丙肝自從索非布韋上市以來治愈率達到99%。Arrowhead公司采用RNA干擾技術的新藥ARC-520二期臨床結果接近于功能性治愈。非酒精脂肪型肝炎藥品的研發也有奧貝膽酸達到了2期臨床終點,并且有超過10個不同靶點在開發中。
在這些藥品的影響下我們預計未來10年全世界肝癌病人的發病率將大幅下降,根據目前的流行病學調查結果所做出的測算根本不具備投資決策的參考價值。那么在A,B兩家公司之間對比明顯A受到的負面影響會更大。因為肝臟作為血流最豐富的臟器之一,是癌癥轉移灶的常見位置,肝臟生理構造使B公司的產品有潛力聯其他合免疫療法成為治療其他腫瘤的手段,這是一個非常有挑戰的思考。
雖然創新藥是一個基于科學驅動的行業,但是在投資中對于商業可行性的考量同樣重要。在目前人類已知的400多種疾病中,其中真正有開發價值的不到其中100種。在工作的過程中我們遇到過太多的研發人員將資源用在無價值的適應癥上或將好的技術用在錯誤的方向,下面的C公司則是一個典型案例。
C公司專注于免疫治療中最新銳的細胞療法,也就是我們所熟知的Car-T。同樣公司創始人也深知產品需要特點避免同質化競爭,所以C公司避開大多數Car-T公司扎堆的血液腫瘤領域,另辟蹊徑的選擇在感染領域運用免疫療法來治療HIV。
C公司團隊來自中國頂尖學術機構,其技術儲備完全有能力支撐產品的大部分開發工作。(我們對于其在細胞治療的CMC能力還存有疑問)。經過跟C公司的交流,根據我們過往走訪Car-T公司取得的經驗我們認為C公司的尷尬之處在于細胞療法高昂的成本與已經慢病化的艾滋病之間有著明顯的商業邏輯的沖突。目前Car-T因為是個性化治療,需要為每一個病人定制化生產細胞。這造成Car-T的生產成本十分高昂而且周期極長,與傳統的小分子藥品或大分子藥品相比處于絕對劣勢。而艾滋病到今天為止已經完成了慢病化的過程,即服用現有藥品可以長時間的控制疾病進程。若艾滋病人堅持按照醫囑使用現有藥品,通常情況下他的預期壽命會超過20年。假設艾滋Car-T的臨床結果僅僅取得與小分子藥類似,或者更好的疾病控制效果,其數十萬的成產成本會讓這個產品毫無商業價值。當時我們的認為除非艾滋Car-T可以治愈艾滋病,讓病人免受每日服藥的痛苦的情況下才有商業價值。 若以治愈艾滋病作為臨床終點,艾滋病Car-T的臨床風險過高,項目的潛在收益根本無法抵消項目自身的風險。
研發產品未來在治療指南中的預期位置在商業價值判斷中也是十分重要的考察點,正面例子就以我們投資的江蘇新元素為例。
當我們細數痛風降尿酸藥品時,我們會發現目前已經上市的藥品有4個,分別為別嘌醇,苯溴馬隆,非布索坦(國內叫非布司他)和Zurampic。其中苯溴馬隆有嚴重肝臟副作用,曾經因肝臟致人死亡導致其在歐洲多國退出市場。非布索坦則在2017年11月被美國FDA發出警告,使用非布索坦的患者對比使用別嘌醇的患者出現急性心梗致死的幾率顯著提高。Zurampic則在上市之初就被FDA給與導致急性腎臟衰竭的黑框警告。別嘌醇是最常用的一線藥品(之全球范圍內),而根據中國通風協會的統計使用別嘌醇的病人僅有不到50%能血尿酸達標。若新元素的ABP-671在臨床中成功表現出其臨床前試驗所展現的低毒性特點,那么所有使用別嘌醇后血尿酸仍然不達標的病人都將是ABP-671的潛在用戶。
新元素治療痛風創新藥
下面是舉反面例子,D,E,F三個公司的主要管線均為應用于糖尿病領域的多靶點藥物,包括了SGLT1/2雙重抑制劑,GLP-1/GPCR等。
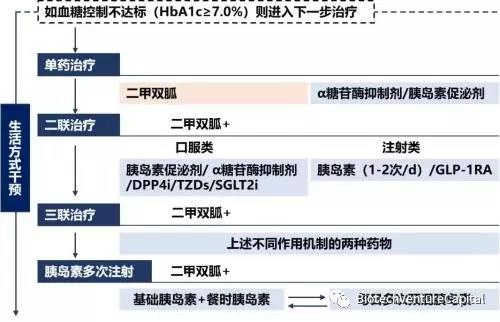
(中國2型糖尿病防治指南2017版)
目前糖尿病指南一線藥物是二甲雙胍和阿卡波糖,二線藥物是DPP-4,GLP-1和SGLT-2等靶點的十余種藥物。自從2007年葛蘭素史克的糖尿病藥物Avandia發現嚴重心血管副作用后,FDA要求所有的糖尿病藥物必須在臨床3期證明其心血管方面的安全性,以保證沒有類似事件再次發生。新的要求造成了三方面重要影響;
(1)糖尿病本身是一種需要長期服藥慢性病,整個臨床試驗的時間拉的非常長。心血管致死事件本身發生幾率就很低,為了得到統計學的顯著差異就要求公司不得不大規模入組病人。這造成了2007年以后的糖尿病藥物3期臨床pivotal試驗動輒組織上千個臨床中心入組1-3萬名病人持續追蹤4-5年,一個3期臨床花費高達數億美金。小型企業根本就不具備組織這類臨床試驗的實力。
(2)自從2007年以來陸續進行3期臨床的糖尿病藥品中有幾種不僅證明了沒有心血管副作用,還證明了這些藥品在心血管方面對比安慰劑有收益。這就造成了未來糖尿病藥品的比拼已經從單純的降糖拓展到了降糖,減肥,降血壓,心血管受益的綜合收益。
(3)2線糖尿病藥品的霸主索馬魯肽的心血管受益機制還不清楚,機制上的不清晰讓讓打敗索馬魯肽更加遙遙無期。
上面這些困難不僅是D,E,F公司要面對的也是目前中國全部研發糖尿病藥品的公司共同面對的問題,如果在臨床上沒有突破或等效那么產品即便上市在指南中也會因為藥效問題排在很多同類藥品之后導致銷售額極低,無法回收投資。
好了,既然是漫談,今天我們暫且聊到這,下期再見。(作者: 郭宇鵬 陳峰)
2021年9月15日,由中山大學腫瘤防治中心主任、院長徐瑞華教授牽頭的特瑞普利單抗聯合化療一線治療復...
 2021-09-15
2021-09-15近日,來自拉丁美洲的一則消息引起了行業廣泛關注:遠大智能工業集團博林特電梯,成功中標哥倫比亞麥德林地...
 2025-02-07
2025-02-07此次賽事不僅是一次足球技藝的較量,更是對香港足球歷史與文化的禮贊,吸引了眾多球迷和媒體的目光。
 2025-02-06
2025-02-06中免海南六大門店聯動,以民俗文化、購物優惠、文旅體驗三重奏,全方位營造熱鬧喜慶的春節氛圍,將免稅購物...
 2025-02-06
2025-02-06投資家網(m.51baobao.cn)是國內領先的資本與產業創新綜合服務平臺。為活躍于中國市場的VC/PE、上市公司、創業企業、地方政府等提供專業的第三方信息服務,包括行業媒體、智庫服務、會議服務及生態服務。長按右側二維碼添加"投資哥"可與小編深入交流,并可加入微信群參與官方活動,趕快行動吧。
